各位实验室同仁、相关机构注意啦!
中国合格评定国家认可委员会(CNAS)对《实验室认可规则》(CNAS-RL01)进行了重要修订,新版CNAS-RL01:2025将于2025年6月30日正式发布,并即日起实施!
本次修订聚焦适用性与可操作性提升,虽未涉及重大结构性调整,但对多项关键内容进行了优化与补充,实验室在申请、运行及管理过程中需重点关注!

一、新版文件获取方式
登录CNAS官网(https://www.cnas.org.cn)→ 进入【认可规范】栏目 → 选择【实验室—认可规则—专用规则】即可查找下载。
二、主要修订内容速览(附重点解读)
|
序号 |
修订要点 |
关键变化 |
影响提示 |
|
1 |
术语定义更新 |
如“授权签字人”新增“直接能力签发带认可标识/声明认可状态报告”的要求;“能力验证”“实验室间比对”等术语同步国际标准(ISO/IEC 17043:2023),删除冗余注释,强调“表现”与“鉴定”环节。 |
申请授权签字人及参与能力验证/比对的实验室需注意新定义下的责任与流程。 |
|
2 |
申请条件细化 |
明确申请人需“自愿申请”,CNAS依据认可准则对申请范围评审并决策,语言更简洁规范。 |
申请流程不变,但需确保申请范围与实际能力严格匹配。 |
|
3 |
评审安排灵活性 |
受理申请后3个月内安排评审,新增“不可抗力因素”作为可延期理由。 |
若遇不可抗力导致延误,实验室可合理说明。 |
|
4 |
评审员公正性要求升级 |
申请人不得拒绝指定评审员的理由,新增“保密性”要求(原仅“公正性”)。 |
实验室需配合评审工作,不得仅以主观理由拒绝评审员。 |
|
5 |
专项监督机制完善 |
新增“专项监督”定义(针对获准认可机构合规性的不定期检查),并允许CNAS邀请无利益冲突的行业权威技术机构协助(仅承担事务性工作)。 |
实验室需重视日常合规管理,避免因合规问题触发专项监督。 |
|
6 |
管理体系运行要求 |
正式运行时间仍为6个月以上,但明确需覆盖“全部场所和能力范围”(原为“申请范围”),文件需具备可操作性。 |
多场所实验室需确保各场所体系均有效运行并符合要求。 |
|
7 |
不予受理再申请限制 |
因诚信等问题被拒后,36个月内不得再次申请,CNAS保留进一步限制权利(原表述为“不再受理”)。 |
诚信问题后果更明确,实验室需珍惜信用记录。 |
|
8 |
测量结果溯源性补充 |
无法溯源至SI单位时,需通过参考物质(RM)标准值、公认方法或实验室间比对证明一致性,优先选择CNAS/APAC/ILAC认可实验室比对。 |
检测结果溯源性要求更具体,比对实验室资质有明确指向。 |
|
9 |
人员兼职限制 |
从事检测/校准/鉴定人员不得“同时在其他实验室兼职”(原为“不得在其他同类型实验室从事同类活动”)。 |
人员管理更严格,避免利益冲突。 |
|
10 |
现场评审中止情形扩展 |
中止评审的情形从7项增至9项(如合并原7.8/7.9条款),新增“多个项目/参数不具备能力”“提供不真实记录”“管理体系失效”等。 |
实验室需全面准备评审材料,确保能力覆盖与记录真实性。 |
|
11 |
变更通知范围扩大 |
获准认可实验室除原“名称/地址/标准/授权签字人”外,新增“最高管理者、法定代表人”变更需提交《变更申请书》,其他信息(如质量/技术负责人)需及时更新。 |
高层管理人员变动也需正式申报! |
|
12 |
处置程序期间限制新增 |
启动能力/资格处置程序后,暂停受理“名称变更、暂停/注销资格、缩小能力范围”等申请(原仅限缩小范围等)。 |
处置期间实验室需谨慎处理其他变更需求。 |
|
13 |
新增义务条款 |
实验室需接受专项监督(新增义务),并在受行政/刑事处罚后20个工作日内书面告知CNAS。 |
合规管理需常态化,处罚信息及时报备。 |
三、重点提醒
过渡安排:新版规则自发布日(2025年6月30日)起立即实施,无缓冲期,请各实验室尽快对照修订内容自查。
核心变化:聚焦术语规范性、评审严谨性、合规管理强化及人员/场所管理细化,实验室需重点关注授权签字人职责、测量溯源性要求、现场评审中止情形及变更申报范围。
文件下载:登录CNAS官网“认可规范-实验室-认可规则-专用规则”栏目,一键获取最新版CNAS-RL01:2025。
结语:规则更新是为了更好地服务实验室高质量发展!建议各机构组织相关人员学习新版规则,确保申请与运行全流程符合最新要求。如有疑问,可随时联系CNAS秘书处或关注官方后续解读。
立即行动:点击CNAS官网(https://www.cnas.org.cn)链接下载新版文件,对照检查,从容应对!
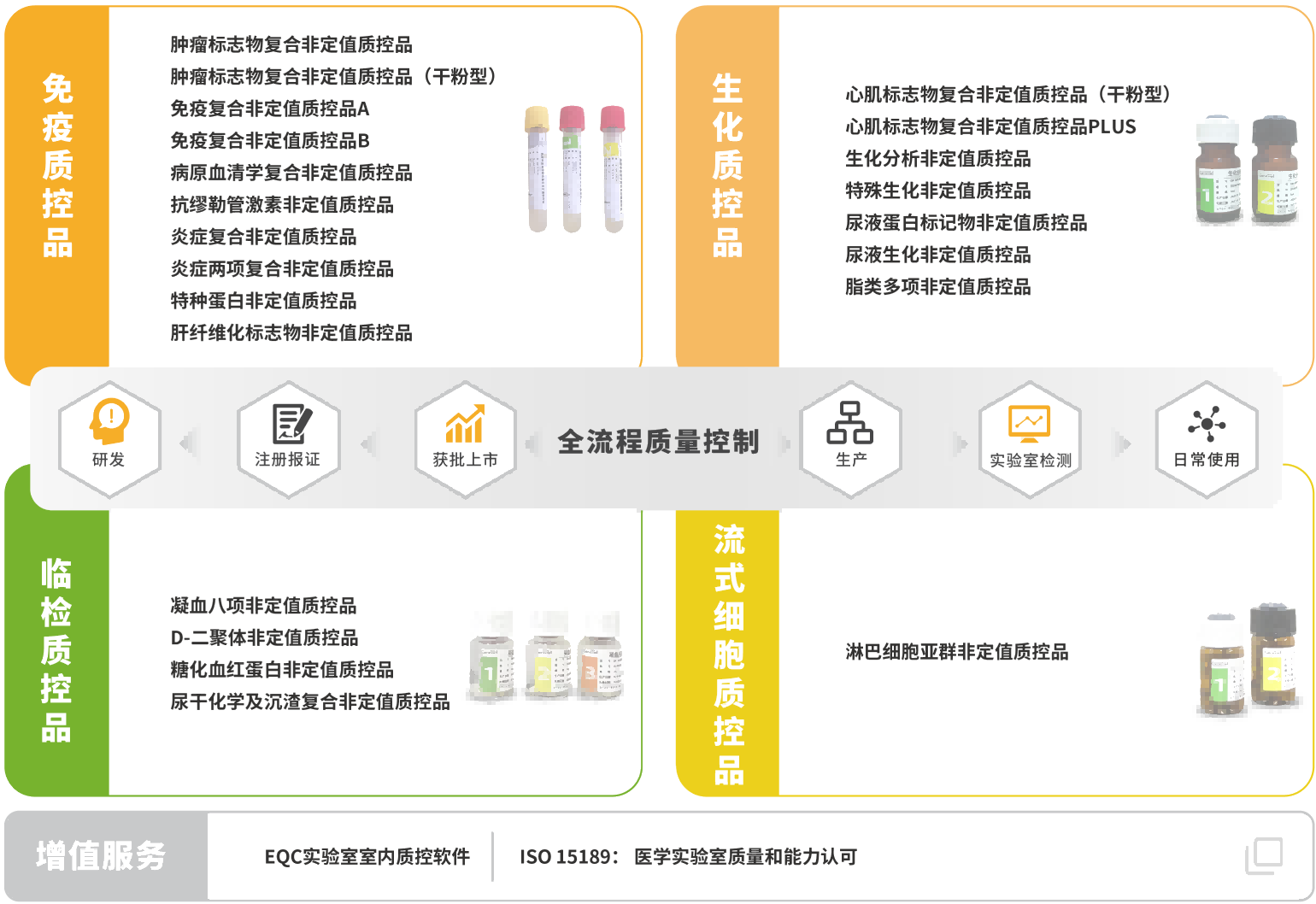
菁良临床质控一站式解决方案
菁良通过自主研发和国产化生产,向体外检测行业用户及合作伙伴提供全球领先的临床实验室质量控制解决方案,协助医学实验室实现全面质量管理。现已推出专业的质控管理软件及ISO15189质量管理体系咨询服务,第三方质控品涵盖免疫诊断、生化诊断、分子诊断等体外诊断细分领域。
关于菁良
菁良科技(深圳)有限公司是全球领先的提供体外诊断标准品与质控品的研发创新型高科技企业。
菁良通过自主研发的平台,向体外检测行业用户及合作伙伴提供全球领先的标准物质、第三方质控产品和企业参考品服务,助力提高行业检测准确率。参与多项由检测领域行业龙头和监管机构发起的标准制定工作,多次支持由临检中心发起的室间质量评价 (EQA)/能力验证项目。
菁良秉承着“精准制标,匠心良造”的理念,怀抱着“提高体外检测准确率,助力精准医学快速发展”的愿景,致力于建立规范化的中国体外检测金标准平台。
